Αίτησης Χορήγησης του νέου αντιϊκου φαρμάκου PAXLOVID σε ασθενείς με COVID-19
Σας ενημερώνουμε ότι από σήμερα Παρασκευή 25-3-2022 ξεκινά η διαδικασία αίτησης χορήγησης του νέου αντιικού φαρμάκου Nirmatrelvir/Ritonavir (PAXLOVID®, PFIZER) σε ασθενείς με COVID-19.
Η αίτηση θα εξακολουθήσει να καταχωρίζεται μέσω της επιλογής «Αίτηση για χορήγηση Αντιικών φαρμάκων σε Ασθενείς με COVID-19» στην ενότητα «Βεβαιώσεις-Πιστοποιητικά- Γνωματεύσεις».
Ο θεράπων ιατρός έχει τη δυνατότητα να υποβάλλει Αίτηση χορήγησης Αντιϊκών φαρμάκων για έναν ασθενή του, εφόσον:
• έχει επιβεβαιωθεί η νόσησή του κατά το τελευταίο τριήμερο είτε με Rapid test είτε με PCR test
• δε νοσηλεύεται και
• πληροί τα κριτήρια που έχουν αποφασιστεί από την Εθνική Επιτροπή Προστασίας της Δημόσιας Υγείας έναντι του κορωνοϊού COVID-19
Λόγω της πιθανότητας για παρουσία αλληλοεπιδράσεων μεταξύ της ριτοναβίρης και φαρμάκων που ήδη λαμβάνει ο ασθενής που είναι υποψήφιος για το PAXLOVID®, συνιστάται να γίνεται έλεγχος για πιθανές αλληλεπιδράσεις ΟΛΩΝ των φαρμάκων που λαμβάνει ο ασθενής, από τον θεράποντα ιατρό, με χρήση του συνδέσμου https://www.covid19-druginteractions.org/.
Δεν απαιτείται συναίνεση του ασθενούς, αλλά απαιτείται ο ασθενής να έχει άυλη συνταγογράφηση, Ως εκ τούτου, απαραίτητη προϋπόθεση για την καταχώρηση της αίτησης είναι ο ασθενής να έχει δηλώσει προηγούμενα ότι επιθυμεί άυλη συνταγογράφηση, μέσω της ενιαίας ψηφιακής πύλης gov.gr.
Μετά την έγκριση χορήγησης του φαρμάκου – για την οποία ενημερώνεται με sms μήνυμα – ο ιατρός θα πρέπει να προχωρήσει στη συνταγογράφηση του φαρμάκου.
Δείτε εδώ https://bit.ly/3JHOzb4 το Δελτίο Τύπου του Υπουργείου Υγείας για τη χορήγηση του νέου αντιϊκού φαρμάκου σε ασθενείς με λοίμωξη COVID-19.
Δείτε κάτωθι ενημέρωση προς επαγγελματίες υγείας από την Pfizer


Η πρώτη από του στόματος αντι-ιική θεραπεία που εγκρίθηκε από την Ευρωπαϊκή Ένωση για τη θεραπεία της COVID-19.1,2
To PAXLOVID κατέδειξε 88,9% μείωση του σχετικού κινδύνου νοσηλειών ή θανάτων, σε σχέση με το εικονικό φάρμακο, σε ενήλικες ασθενείς με αυξημένο κίνδυνο εξέλιξης σε σοβαρή νόσο COVID-19, που ξεκίνησαν θεραπεία εντός 3 ημερών από την έναρξη των συμπτωμάτων (p<0,001).3
Το PAXLOVID ενδείκνυται για τη θεραπεία της νόσου του κορωνοϊού 2019 (COVID-19) σε ενήλικες για τους οποίους δεν απαιτείται συμπληρωματική χορήγηση οξυγόνου και οι οποίοι έχουν αυξημένο κίνδυνο εξέλιξης σε σοβαρή νόσο COVID-19.1Διαβάστε περισσότερες πληροφορίες για το PAXLOVID
Δοσολογία1
Δύο φορές ημερησίως (κάθε 12 ώρες) για 5 συνεχόμενες ημέρες
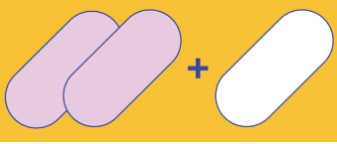
Πρωϊνή δόση
• Δύο ροζ δισκία των 150 mg PF-07321332
• Ένα λευκό δισκίο των 100 mg ριτοναβίρης
Οι ασθενείς πρέπει να λαμβάνουν και τα 3 δισκία μαζί

Βραδινή δόση
• Δύο ροζ δισκία των 150 mg PF-07321332
• Ένα λευκό δισκίο των 100 mg ριτοναβίρης
Οι ασθενείς πρέπει να λαμβάνουν και τα 3 δισκία μαζί
• Το PAXLOVID μπορεί να ληφθεί με ή χωρίς τροφή.
• Τα δισκία θα πρέπει να καταπίνονται ολόκληρα και να μην μασώνται, να μην σπάζουν και να μην συνθλίβονται, καθώς δεν υπάρχουν προς το παρόν διαθέσιμα δεδομένα.
Για το πλήρες κείμενο της δοσολογίας και του τρόπου χορήγησης συμβουλευτείτε την Περίληψη Χαρακτηριστικών του Προϊόντος.
Βιβλιογραφία :
1. PAXLOVID Περίληψη Χαρακτηριστικών Προϊόντος 01/2022. 2. COVID-19: EMA recommends conditional marketing authorisation for Paxlovid. Διαθέσιμο σε: https:// www. ema.europa. eu/en/news/ covid-19-ema-recommends-conditional-marketing-authorisation-Paxlovid (Τελευταία πρόσβαση Φεβρουάριος 2022). 3. Hammond et al. 2022. N Engl J Med. DOI: 10.1056/NEJMoa2118542.
ΣΗΜΑΝΤΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ ΑΣΦΑΛΕΙΑΣ1

• To Paxlovid αντενδείκνυται σε ασθενείς με υπερευαισθησία στις δραστικές ουσίες ή σε οποιοδήποτε από τα έκδοχα, σε ασθενείς που λαμβάνουν φαρμακευτικά προϊόντα των οποίων η κάθαρση εξαρτάται σε μεγάλο βαθμό από το CYP3A και για τα οποία οι αυξημένες συγκεντρώσεις σχετίζονται με σοβαρές ή/και απειλητικές για τη ζωή αντιδράσεις και σε ασθενείς με φαρμακευτικά προϊόντα που είναι ισχυροί επαγωγείς του CYP3A, όπου οι σημαντικά μειωμένες συγκεντρώσεις του Paxlovid στο πλάσμα μπορεί να σχετίζονται με το ενδεχόμενο απώλειας της ιολογικής ανταπόκρισης και πιθανή αντοχή. Για περαιτέρω πληροφορίες, συμβουλευθείτε την Περίληψη Χαρακτηριστικών του Προϊόντος του Paxlovid ή ανατρέξτε στην ηλεκτρονική σελίδα https://www.covid19oralrx.com.
• Η ασφάλεια και η αποτελεσματικότητα του Paxlovid σε ασθενείς ηλικίας κάτω των 18 ετών δεν έχουν τεκμηριωθεί. Το Paxlovid δεν θα πρέπει να χρησιμοποιείται σε ασθενείς με σοβαρή ηπατική δυσλειτουργία και σε ασθενείς με σοβαρή νεφρική δυσλειτουργία [eGFR < 30 mL/min, συμπεριλαμβανομένων των ασθενών με Νεφρική Νόσο Τελικού Σταδίου (ESRD) υπό αιμοκάθαρση]. Σε ασθενείς με μέτρια νεφρική δυσλειτουργία (eGFR ≥ 30 έως < 60 mL/min), η δόση του Paxlovid θα πρέπει να μειωθεί σε PF-07321332/ριτοναβίρη 150 mg/100 mg, κάθε 12 ώρες για 5 ημέρες ώστε να αποφευχθεί η υπερέκθεση (αυτή η προσαρμογή δόσης δεν έχει δοκιμαστεί κλινικά). Συνεπώς, οι ασθενείς με μέτρια νεφρική δυσλειτουργία θα πρέπει να προειδοποιούνται σχετικά με το γεγονός ότι θα πρέπει να λαμβάνουν μόνο ένα δισκίο PF-07321332 μαζί με το δισκίο ριτοναβίρης κάθε 12 ώρες.
• Η συνιστώμενη δοσολογία είναι 300 mg PF-07321332 (δύο δισκία των 150 mg) με 100 mg ριτοναβίρης (ένα δισκίο των 100 mg), τα οποία λαμβάνονται όλα μαζί από του στόματος κάθε 12 ώρες επί 5 ημέρες. Το Paxlovid θα πρέπει να χορηγείται όσο το δυνατόν συντομότερα μετά από τη διάγνωση της νόσου COVID-19 και εντός 5 ημερών από την έναρξη των συμπτωμάτων. Συνιστάται η ολοκλήρωση του πλήρους κύκλου θεραπείας 5 ημερών, ακόμη και αν ο ασθενής χρειαστεί νοσηλεία λόγω σοβαρής ή κρίσιμης μορφής νόσου COVID-19 μετά την έναρξη της θεραπείας με Paxlovid.
• Εάν ο ασθενής παραλείψει μια δόση του Paxlovid εντός 8 ωρών από την ώρα που συνήθως λαμβάνεται, ο ασθενής θα πρέπει να τη λάβει το συντομότερο δυνατό και να συνεχίσει το κανονικό πρόγραμμα χορήγησης δόσεων. Εάν ο ασθενής παραλείψει μια δόση για περισσότερες από 8 ώρες, ο ασθενής δεν θα πρέπει να λάβει τη δόση που παραλείφθηκε αλλά να λάβει την επόμενη δόση κατά την κανονικά προγραμματισμένη ώρα. Ο ασθενής δεν θα πρέπει να πάρει διπλή δόση για να αναπληρώσει τη δόση που έχει παραλειφθεί.
• Σε ασθενείς που λαμβάνουν ριτοναβίρη έχουν παρουσιαστεί αυξήσεις των ηπατικών τρανσαμινασών, κλινική ηπατίτιδα και ίκτερος. Ως εκ τούτου, θα πρέπει να δίνεται προσοχή κατά τη χορήγηση του Paxlovid σε ασθενείς με προϋπάρχουσες ηπατικές παθήσεις, διαταραχές των ηπατικών ενζύμων ή ηπατίτιδα.
• Επειδή το PF-07321332 συγχορηγείται με ριτοναβίρη, ενδέχεται να υπάρχει κίνδυνος ανάπτυξης αντοχής του HIV-1 στους αναστολείς πρωτεάσης του HIV σε άτομα με μη ελεγχόμενη ή αδιάγνωστη λοίμωξη από HIV-1.
• Το Paxlovid είναι ένας αναστολέας του CYP3A και μπορεί να αυξήσει τις συγκεντρώσεις στο πλάσμα των φαρμακευτικών προϊόντων που μεταβολίζονται κυρίως από το CYP3A. Η έναρξη φαρμακευτικών προϊόντων που αναστέλλουν ή επάγουν το CYP3A ενδέχεται να αυξήσει ή να μειώσει τις συγκεντρώσεις του Paxlovid, αντίστοιχα. Για τους παραπάνω λόγους, θα πρέπει να εξετάζεται το ενδεχόμενο δυνητικά σημαντικών αλληλεπιδράσεων με άλλα φαρμακευτικά προϊόντα πριν και κατά τη διάρκεια της θεραπείας με Paxlovid, προκειμένου να ελαχιστοποιηθεί ο κίνδυνος σοβαρών ανεπιθύμητων ενεργειών. Ως συντηρητικό μέτρο, οι φαρμακευτικές αλληλεπιδράσεις που αφορούν στη ριτοναβίρη που χρησιμοποιείται στη χρόνια λοίμωξη από HIV (600 mg 2 φορές ημερησίως όταν χρησιμοποιήθηκε αρχικά ως αντιρετροϊκός παράγοντας και 100 mg 2 φορές ημερησίως όπως χρησιμοποιείται επί του παρόντος ως φαρμακοκινητικός ενισχυτής με αντιρετροϊκούς παράγοντες), θα πρέπει να εφαρμόζονται για το Paxlovid. Μελλοντικές έρευνες ενδέχεται να επιτρέψουν την προσαρμογή των συστάσεων που σχετίζονται με τις φαρμακευτικές αλληλεπιδράσεις στη θεραπεία διάρκειας 5 ημερών με το Paxlovid. Για περαιτέρω πληροφορίες, συμβουλευθείτε την Περίληψη Χαρακτηριστικών του Προϊόντος του Paxlovid ή ανατρέξτε στην ηλεκτρονική σελίδα https://www.covid19oralrx.com.
• Το Paxlovid δεν συνιστάται κατά τη διάρκεια της εγκυμοσύνης και σε γυναίκες σε αναπαραγωγική ηλικία που δεν χρησιμοποιούν μια αποτελεσματική μέθοδο αντισύλληψης, εκτός εάν οι κλινικές συνθήκες απαιτούν θεραπεία με Paxlovid. Δεν υπάρχουν δεδομένα σχετικά με τη χρήση του Paxlovid σε έγκυες γυναίκες και σε γυναίκες που θηλάζουν. Ο θηλασμός θα πρέπει να διακόπτεται προσωρινά κατά τη διάρκεια της θεραπείας και ως προληπτικό μέτρο για 7 ημέρες μετά τη συμπλήρωση της θεραπείας με Paxlovid. Οι γυναίκες σε αναπαραγωγική ηλικία θα πρέπει να αποφύγουν να μείνουν έγκυες κατά τη διάρκεια της θεραπείας με Paxlovid και ως προληπτικό μέτρο για 7 ημέρες μετά από την ολοκλήρωση της θεραπείας με Paxlovid. Η χρήση της ριτοναβίρης μπορεί να μειώσει την αποτελεσματικότητα των συνδυασμένων ορμονικών αντισυλληπτικών. Οι ασθενείς που χρησιμοποιούν συνδυασμένα ορμονικά αντισυλληπτικά θα πρέπει να λαμβάνουν οδηγίες να χρησιμοποιούν μια αποτελεσματική εναλλακτική μέθοδο αντισύλληψης ή μια πρόσθετη μέθοδο αντισύλληψης φραγμού κατά τη διάρκεια της θεραπείας με Paxlovid και μέχρι έναν έμμηνο κύκλο μετά τη διακοπή του Paxlovid.
• Οι πιο συχνές ανεπιθύμητες ενέργειες, που αναφέρθηκαν κατά τη διάρκεια της θεραπείας με δισκία Paxlovid κάθε 12 ώρες επί 5 ημέρες και κατά τη διάρκεια 34 ημερών μετά την τελευταία δόση ήταν δυσγευσία (5,6%), διάρροια (3,1%), κεφαλαλγία (1,4%) και έμετος (1,1%).Για το πλήρες κείμενο της δοσολογίας και του τρόπου χορήγησης συμβουλευτείτε την Περίληψη Χαρακτηριστικών του Προϊόντος.
Για την Περίληψη Χαρακτηριστικών του Προϊόντος Paxlovid πατήστε εδώ.
Το παρόν απευθύνεται αυστηρά σε επαγγελματίες υγείας. Οποιαδήποτε προώθηση του παρόντος ή κοινοποίηση του περιεχομένου του σε μη επαγγελματία υγείας απαγορεύεται ρητά και ο αποστολέας δε φέρει καμία ευθύνη.
Το παρόν σας αποστέλλεται διότι δηλώσατε ενδιαφέρον να λαμβάνετε μηνύματα ηλεκτρονικής ενημέρωσης από την Pfizer. Σε περίπτωση που επιθυμείτε να διαγραφείτε από τη λίστα παραληπτών των εν λόγω ηλεκτρονικών μηνυμάτων, παρακαλούμε πατήστε εδώ.
Pfizer Ελλάς Α.Ε., Λ. Μεσογείων 243, Ν. Ψυχικό 154 51, Αθήνα, Ελλάδα, Τηλ. Επικοινωνίας 210-6785800
Αριθ. Γ.Ε.ΜΗ. 000242901000
PP-PAX-GRC-0009-MAR22

| Βοηθήστε να γίνουν τα φάρμακα πιο ασφαλή και Αναφέρετε ΟΛΕΣ τις ανεπιθύμητες ενέργειες για ΟΛΑ τα φάρμακα Συμπληρώνοντας την «ΚΙΤΡΙΝΗ ΚΑΡΤΑ» |